Partikel Penyusun Atom, Bilangan Kuantum dan Konfigurasi Elektron
A. Partikel Penyusun Atom
Partikel penyusun atom terdiri dari Proton, elektron dan neutron.
1. Proton
Jumlah proton yang terdapat dalam inti atom dikenal sebagai nomor atom unsur. Massa atom terkonsentrasi pada inti yang terdiri dari proton dan neutron. Massa proton dan neutron hampir sama, namun itu sekitar 1.836 kali lebih berat daripada elektron. Muatan positif antara proton menyebabkan mereka saling tolak. Sebuah gaya nuklir yang kuat mengikat proton bersama-sama. Gaya ini diberikan oleh keberadaan 1 quark bawah dan 2 quark atas dalam proton.
- Muatan pada proton = 2 (⅔) + (- ⅓) = 1.
- Dengan demikian, proton memperoleh muatan positif
2. Elektron
Ditemukan oleh JJ. Thomson pada tahun 1897, sebuah elektron adalah partikel subatomik yang paling ringan yang terikat ke inti dengan gaya tarik-menarik antara elektron negatif dan proton yang bermuatan positif. Sebagian besar atom adalah ruang kosong di mana elektron mengorbit di sekitar inti dan mencoba untuk mencapai keadaan stabil. Elektron memainkan peran penting dalam banyak fenomena fisik seperti listrik, magnet dan konduktivitas termal.
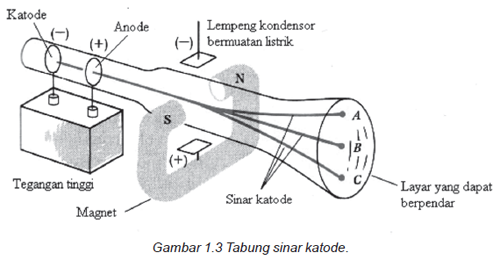
Thomson melakukan percobaan dengan menggunakan tabung sinar katode. Terdapat dua plat elektroda dimana salah satu plat logam yang terdapat pada ujung tabung berfungsi sebagai katoda. Kedua plat ini dimasukkan ke dalam tabung kaca bertekanan rendah kemudian dialirkan listrik bertegangan tinggi hingga mampu melepas elektron dari katoda ke anoda.
Sinar katoda tidak dapat kita lihat menggunakan mata telanjang namun kita bisa mengetahui bahwa sinar ini ada dari berpenjarnya lapisan tabung kaca bagian dalam akibat adanya benturan antara elektron dengan dinding tabung. Atau kita bisa melihatnya jika sinar katoda kita benturkan ke layar ber-fluoresensi (layar yang dapat berpendar) setelah terlebih dahulu kita beri lubang pada plat logam anoda. Seperti gambar di bawah ini.
Dari hasil percobaannya ditemukan sifat sinar katode yaitu:
- Merupakan radiasi partikel karena mampu memutar baling-baling.
- Radiasi ini bila dibelokkan menggunakan medan magnet, maka akan menuju ke kutub magnet positif. Itu artinya sinar katode bermuatan negatif.
- Partikel katoda merambat tegak lurus dari lempengan katode menuju anode.
- Sinar katoda tidak tergantung pada jenis plat logam yang digunakan.
- Sinar katoda dapat kita buat dengan listrik tegangan tinggi.
Dari sifat inilah kemudian oleh J.J Thomson menamakan partikel penyusun atom bermuatan negatif ini sebagai elektron. Setelain ini J.J Thomson juga menemukan perbandingan muatan elektron terhadap massa yaitu 1,76 × 108 C/g yang kemudian pada tahun 1909, Robert Millikan berhasil menemukan besarnya muatan sebuah elektron yaitu 1,6 × 10-19 C. Dengan demikian, maka kita peroleh massa 1 elektron sebesar 9,1095×10-31 Kg.
3. Neutron
Neutron tidak memiliki muatan atau netral dan pada tahun 1932, seorang ahli fisika Inggris James Chadwick menemukan bahwa itu terletak pada inti. Neutron lebih lanjut terdiri dari partikel fundamental yang disebut quark. Hal ini terdiri dari 1 ke atas dan 2 quark ke bawah. Quark membawa nilai pecahan muatan dan karenanya menentukan muatan partikel.
- 1 quark atas = muatan ⅔ e dan quark bawah = muatan – ⅓ e.
- Oleh karena itu muatan neutron = ⅔ + (- ⅓ – ⅓) = 0.
- Dengan demikian, neutron tidak memiliki muatan.
B. Bilangan Kuantum
Bilangan kuantum (dalam fungsi gelombang) adalah bilangan yang memiliki makna khusus dalam menjelaskan keadaan sistem kuantum. Bilangan-bilangan kuantum dapat memberikan deskripsi keadaan elektron dalam atom.
Setelah dikemukakannya teori dualisme partikel−gelombang, pada tahun 1926 Erwin Schrödinger mengajukan teori mekanika kuantum yang menjelaskan struktur atom. Model atom mekanika kuantum Schrödinger dinyatakan dalam persamaan matematis yang disebut persamaan gelombang. Penyelesaian persamaan gelombang Schrödinger untuk atom hidrogen menghasilkan fungsi gelombang (ψ) atau orbital atom yang menggambarkan keberadaan elektron dalam atom. Kuadrat dari fungsi gelombang, ψ2, memiliki arti khusus yaitu besar probabilitas menemukan elektron dalam ruang dengan volum tertentu di sekitar inti atom. Sebagaimana asas ketidakpastian Heisenberg, posisi elektron dalam atom tidak dapat dipastikan, namun hanya dapat diketahui tempat di mana elektron paling mungkin ditemukan.
1. Orbital Bilangan Kuantum
Setiap orbital atom memiliki satu set tiga bilangan kuantum yang unik, antara lain bilangan kuantum utama (n), azimuth (atau momentum angular) (l), dan magnetik (ml). Ketiga bilangan kuantum tersebut dapat mendeskripsikan tingkat energi orbital dan juga ukuran, bentuk, dan orientasi dari distribusi probabilitas radial orbital atom. Lalu, terdapat bilangan yang keempat, yakni bilangan kuantum spin (ms), yang memberikan informasi spin suatu elektron dalam sebuah orbital. Setiap elektron dalam sebuah atom memiliki satu set empat bilangan kuantum yang unik, yakni n, l, ml, dan ms.
- Bilangan kuantum utama (n) mendeskripsikan ukuran dan tingkat energi orbital. Semakin besar nilai n, maka semakin besar ukuran orbital dan semakin tinggi tingkat energinya. Nilai n yang diperbolehkan adalah bilangan bulat positif (1, 2, 3, dan seterusnya).
- Bilangan kuantum azimuth (l) mendeskripsikan bentuk orbital. Nilai l yang diperbolehkan adalah bilangan bulat dari 0 hingga n − 1.
- Bilangan kuantum magnetik (ml) mendeskripsikan orientasi orbital. Nilai ml yang diperbolehkan adalah bilangan bulat dari −l hingga +l.
- Bilangan kuantum spin (ms) mendeskripsikan arah spin elektron dalam orbital. Nilai ms yang diperbolehkan adalah +½ atau −½.
Kombinasi bilangan kuantum n, l, dan ml yang mungkin pada 4 kulit elektron pertama dapat dilihat pada tabel berikut:
2. Bentuk Orbital Atom
a). Orbital s
Orbital s adalah orbital dengan l = 0 berbentuk bola dengan inti atom pada bagian tengah. Oleh karena bola hanya memiliki satu orientasi, semua orbital s hanya memiliki satu nilai ml, yaitu ml = 0. Orbital 1s memiliki densitas (kerapatan) elektron tertinggi pada bagian inti atom dan kemudian densitas semakin menurun perlahan-lahan setelah menjauh dari inti atom. Orbital 2s memiliki dua daerah dengan densitas elektron tinggi. Di antara kedua daerah tersebut terdapat simpul bola, di mana probabilitas menemukan elektron pada daerah tersebut menurun hingga nol (ψ2 = 0). Pada orbital 3s, terdapat tiga daerah dengan densitas elektron tinggi dan dua simpul. Pola bertambahnya simpul orbital s ini masih terus berlanjut dengan orbital 4s, 5s, dan seterusnya.
b). Orbital p
Orbital p adalah orbital dengan l = 1 berbentuk seperti balon terpilin dengan dua cuping. Kedua cuping terletak pada dua sisi inti atom yang saling bersebrangan. Inti atom terletak pada bidang simpul orbital p, yakni di antara dua cuping yang masing-masing memiliki densitas elektron tinggi. Orbital p memiliki tiga jenis orientasi ruang, px, py, dan pz, sebagaimana terdapat tiga nilai ml yang mungkin, yaitu −1, 0, atau +1. Ketiga orbital p tersebut terletak saling tegak lurus pada sumbu x, y, dan z koordinat Kartesius dengan bentuk, ukuran, dan energi yang sama.

3). Orbital d
Orbital d adalah orbital dengan l = 2. Orbital d memiliki lima jenis orientasi, sebagaimana terdapat lima nilai ml yang mungkin, yaitu −2, −1, 0, +1, atau +2. Empat dari lima orbital d, antara lain dxy, dxz dyz, dan dx2−y2, memiliki empat cuping seperti bentuk daun semanggi. Orbital d kelima, dz2, memiliki dua cuping utama pada sumbu z dan satu bagian berbentuk donat pada bagian tengah.

4). Orbital f
Orbital f adalah orbital dengan l = 3. Orbital f memiliki tujuh jenis orientasi, sebagaimana terdapat tujuh nilai ml yang mungkin (2l + 1 = 7). Ketujuh orbital f memiliki bentuk yang kompleks dengan beberapa cuping.

C. Konfigurasi elektron
Setelah memahami hubungan keberadaan elektron dalam atom dengan orbital pada teori atom mekanika kuantum, berikut akan dibahas konfigurasi elektron, yaitu penyusunan elektron-elektron dalam orbital-orbital pada kulit-kulit atom multi elektron. Aturan-aturan dalam penentuan konfigurasi elektron berdasarkan orbital, antara lain:
- Asas Aufbau: Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit yang terlihat pada gambar berikut.

Urutan tingkat energi subkulit
- Asas larangan Pauli: Tidak ada dua elektron dalam satu atom yang memiliki keempat bilangan kuantum yang sama. Setiap orbital maksimum diisi oleh 2 elektron yang memiliki spin yang berlawanan (ms = +½ dan ms = −½).
- Kaidah Hund: Jika ada orbital dengan tingkat energi yang sama, konfigurasi elektron dengan energi terendah adalah dengan jumlah elektron tak berpasangan dengan spin paralel yang paling banyak.

Diagram orbital dan konfigurasi elektron berdasarkan orbital dari 10 unsur pertama
Berdasarkan eksperimen, terdapat anomali konfigurasi elektron dari aturan-aturan di atas. Subkulit d memiliki kecenderungan untuk terisi setengah penuh atau terisi penuh. Contohnya, konfigurasi elektron 24Cr: [Ar] 4s1 3d5 lebih stabil dibanding [Ar] 4s2 3d4; dan 29Cu: [Ar] 4s1 3d10 lebih stabil dibanding [Ar] 4s2 3d9..
Konfigurasi elektron untuk ion monoatomik (seperti Na+, K+, Ca2+, S2-, Br–) dapat ditentukan dari konfigurasi elektron atom netralnya terlebih dahulu. Pada kation (ion bermuatan positif) monoatomik Ax+ yang bermuatan x+, sebanyak x elektron dilepas (dikurangi) dari kulit elektron terluar atom netral A. Pada anion (ion bermuatan negatif) monoatomik By− yang bermuatan y−, sebanyak y elektron ditangkap (ditambahkan) pada orbital level energi terendah yang masih belum penuh oleh elektron.
Daftar Pustaka
https://www.studiobelajar.com/bilangan-kuantum/
https://www.siswapedia.com/partikel-penyusun-atom/
https://usaha321.net/pertikel-penyusun-atom.html
_MCC-21_
Daftar Pustaka
https://www.studiobelajar.com/bilangan-kuantum/
https://www.siswapedia.com/partikel-penyusun-atom/
https://usaha321.net/pertikel-penyusun-atom.html
_MCC-21_







Baguss
BalasHapuskembangkan lagi kakk buat blog nya,, sejaug ini sudah baguss
BalasHapusGood jobbb megaa
BalasHapuswah, update lagi ya kak?.. good good good
BalasHapusMantap mantappp ..
BalasHapusbaguss kak,, bermanfaattt untukkk pelajaran kimiaaa saya
BalasHapusGood jobb mar��
BalasHapus👍👍👍
BalasHapussangat membantu
BalasHapusMannntapppp
BalasHapusMantepp
BalasHapusGuddd👍🏻👍🏻👍🏻
BalasHapusMantap nii👌
BalasHapusMantul³
BalasHapusmantapp
BalasHapusGood maria megaa🐣🐣
BalasHapusKereen kak
BalasHapusKeren kak👍
BalasHapusGoodd
BalasHapusbermnfaat
BalasHapus👍👍👍
BalasHapusKeren
BalasHapusGood👍
BalasHapusGood👌
BalasHapusSangat membantuu
BalasHapus